L’INTESTINO COME ORGANO REGOLATORE SISTEMICO
L’INTESTINO COME ORGANO REGOLATORE SISTEMICO: barriera mucosale, microbiota e implicazioni clinico-nutrizionali
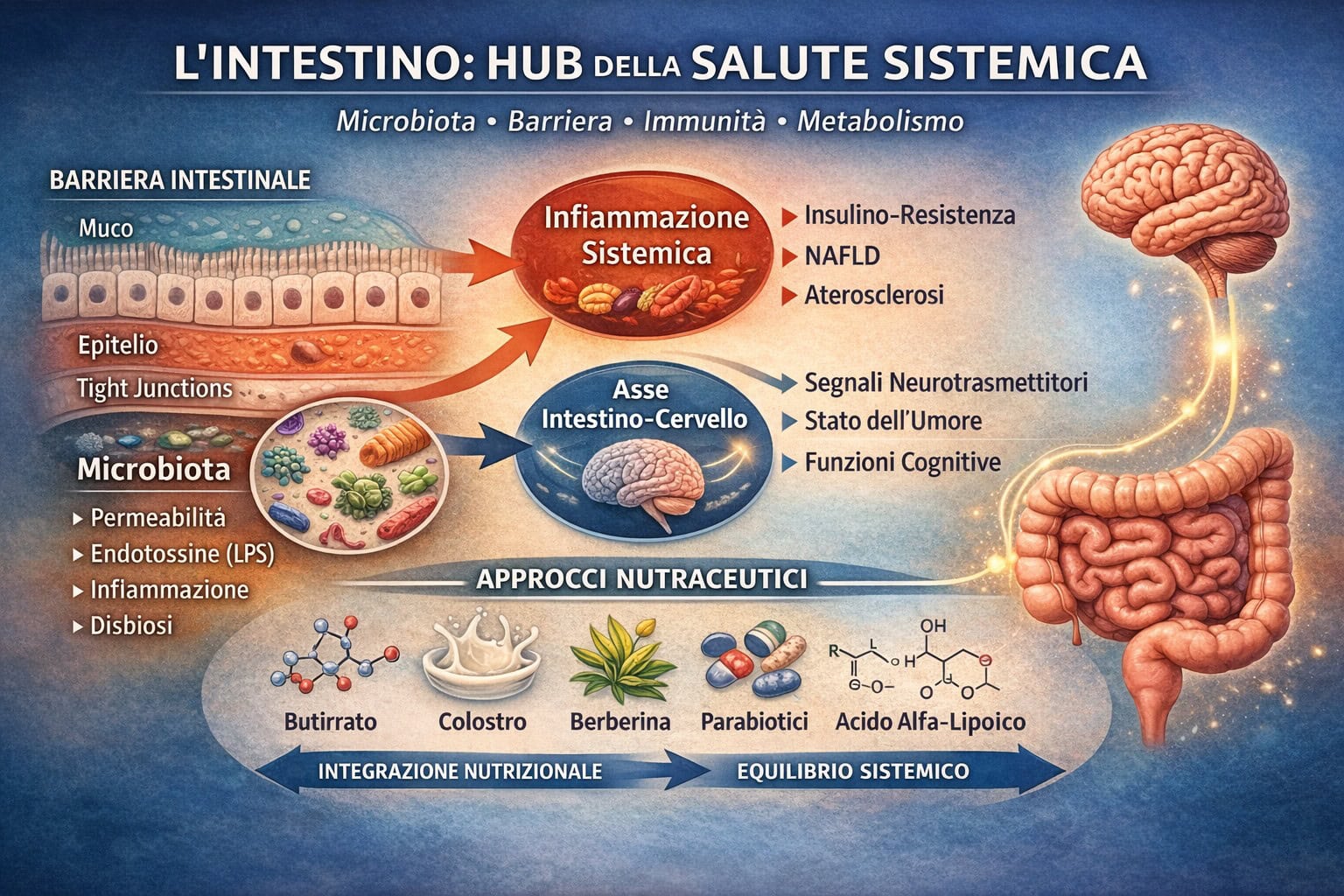
L’intestino come organo regolatore sistemico
Barriera intestinale, microbiota, muco e nutraceutici di supporto: butirrato, berberina, acido alfa-lipoico, colostro bovino e parabiotici
Articolo a cura del Biologo Nutrizionista — aggiornamento divulgativo basato su evidenze indicizzate in PubMed.
In sintesi: la salute intestinale dipende dall’integrazione tra microbiota intestinale, strato di muco, tight junctions e immunità mucosale.
La disfunzione di uno o più livelli può contribuire a infiammazione sistemica e dismetabolismo (Bischoff et al., 2014; Tilg & Moschen, 2014).
Introduzione
Nel panorama della nutrizione clinica contemporanea, l’intestino ha progressivamente assunto un ruolo centrale che trascende la funzione digestivo-assorbitiva tradizionalmente attribuitagli.
L’evidenza scientifica accumulata negli ultimi due decenni descrive l’ecosistema intestinale come una struttura biologica complessa, dotata di funzioni metaboliche, immunologiche e neuroendocrine integrate.
In questa prospettiva, il tratto gastrointestinale può essere considerato una vera e propria interfaccia dinamica tra ambiente esterno e omeostasi interna, capace di modulare processi infiammatori sistemici,
metabolismo energetico e regolazione immunitaria (Bischoff et al., 2014; Tilg & Moschen, 2014).
Architettura funzionale della barriera intestinale
La barriera intestinale non è riconducibile a un singolo elemento anatomico, bensì a un sistema multistrato composto da componenti strutturali e funzionali interdipendenti.
Una lettura utile in ambito clinico-nutrizionale considera quattro livelli principali:
-
Microbiota intestinale
La comunità microbica residente svolge funzioni metaboliche essenziali, tra cui la fermentazione delle fibre alimentari con produzione di acidi grassi a corta catena (SCFA),
la sintesi vitaminica e la modulazione del sistema immunitario mucosale (Kho & Lal, 2018). -
Strato di muco intestinale
Costituito prevalentemente da mucine (in particolare MUC2), rappresenta la prima barriera fisico-chimica contro l’adesione batterica all’epitelio.
Alterazioni qualitative o quantitative di questo strato sono state associate a condizioni infiammatorie croniche intestinali (Johansson et al., 2013). -
Epitelio e tight junctions
Le tight junctions regolano selettivamente la permeabilità paracellulare.
Proteine come occludina, claudine e ZO-1 costituiscono il complesso giunzionale, la cui disfunzione è implicata nell’aumento della permeabilità intestinale (Turner, 2009). -
Immunità mucosale (GALT)
Il tessuto linfoide associato all’intestino (GALT) rappresenta una delle principali componenti immunitarie dell’organismo, con un ruolo chiave nella tolleranza antigenica e nella difesa contro patogeni (Mowat & Agace, 2014).
Nota metodologica: nella pratica clinica, intervenire su un singolo livello raramente è sufficiente; l’efficacia aumenta quando la strategia supporta anche muco, giunzioni epiteliali e immunità mucosale.
Permeabilità intestinale e infiammazione sistemica
L’alterazione dell’integrità della barriera intestinale può determinare il passaggio trans-epiteliale di componenti microbiche, tra cui lipopolisaccaridi (LPS), nel circolo sistemico.
Questo fenomeno, definito endotossiemia metabolica, è stato associato allo sviluppo di infiammazione cronica di basso grado e a condizioni quali obesità, insulino-resistenza, steatosi epatica non alcolica e patologie cardiovascolari (Cani et al., 2007; Hotamisligil, 2006).
In questo contesto, l’intestino agisce come modulatore dell’asse immuno-metabolico sistemico: la barriera non è soltanto un confine anatomico, ma un regolatore funzionale della risposta infiammatoria.
SCFA e butirrato: ruolo sulla mucosa e sull’immunità
Tra i metaboliti microbici maggiormente studiati, gli SCFA (acetato, propionato e butirrato) rappresentano un punto di convergenza tra dieta, microbiota e funzione di barriera.
In particolare, il butirrato si distingue per il suo ruolo energetico sui colonociti e per effetti immunomodulanti mediati anche dall’inibizione delle HDAC (Peng et al., 2009; Furusawa et al., 2013).
Nutraceutici e strategie di supporto alla barriera intestinale
Di seguito vengono descritti alcuni composti con razionale biologico rilevante sul piano intestinale e sistemico.
L’obiettivo è fornire una lettura funzionale, utile al biologo nutrizionista per integrare in modo coerente intervento alimentare, stile di vita e nutraceutica mirata.
Butirrato (acido butirrico)
Razionale biologico: principale fonte energetica per i colonociti; supporto alla differenziazione epiteliale e alle tight junctions (Peng et al., 2009).
Effetto immunomodulante con promozione di linfociti T regolatori (Furusawa et al., 2013).
- Obiettivo funzionale: rinforzo della barriera, modulazione dell’infiammazione mucosale.
- Approccio integrato: priorità a fibre e alimenti fermentabili tollerati, con eventuale supporto nutraceutico in profili selezionati.
- Attenzione clinica: in soggetti con iperfermentazione/IBS o sensibilità gastrointestinale, modulare carico fermentabile e timing.
Berberina
Razionale biologico: proprietà antimicrobiche e antinfiammatorie, con effetti sulla modulazione del microbiota e sulla riduzione di segnali associati all’endotossiemia metabolica (Habtemariam, 2020).
- Obiettivo funzionale: supporto al riequilibrio dell’ecosistema intestinale e modulazione di vie pro-infiammatorie in contesti dismetabolici.
- Approccio integrato: sempre associata a strategia dietetica (fibre, polifenoli, qualità dei grassi) e stile di vita.
- Attenzione clinica: valutare tollerabilità gastrointestinale e possibili interazioni con terapie in corso.
Acido alfa-lipoico (ALA)
Razionale biologico: cofattore mitocondriale con azione antiossidante, in grado di contribuire alla riduzione dello stress ossidativo sistemico
che può concorrere al danno della barriera (Packer et al., 1995).
- Obiettivo funzionale: riduzione del carico ossidativo/infiammatorio sistemico in profili selezionati.
- Approccio integrato: utile quando il dismetabolismo e lo stress ossidativo rappresentano driver clinici.
- Attenzione clinica: personalizzare in base a quadro clinico, farmaci e tollerabilità.
Colostro bovino
Razionale biologico: elevata concentrazione di immunoglobuline, lattoferrina e fattori di crescita (IGF-1, TGF-β).
Studi clinici indicano un potenziale ruolo nel supporto della riparazione mucosale e nella riduzione della permeabilità intestinale, in particolare in condizioni di stress fisiologico elevato (Playford et al., 2001).
- Obiettivo funzionale: supporto trofico e immunologico della mucosa.
- Attenzione clinica: considerare allergie alle proteine del latte e sensibilità individuali.
Moringa oleifera
Razionale biologico: fitocomplesso ricco di polifenoli e isotiocianati con attività antiossidante e modulante NF-κB, contribuendo alla regolazione dell’infiammazione mucosale (Leone et al., 2015).
- Obiettivo funzionale: supporto antiossidante e modulazione dell’infiammazione a bassa intensità.
- Approccio integrato: coerente con pattern alimentari ricchi di polifenoli e fibre.
Parabiotici
Razionale biologico: microrganismi inattivati che non colonizzano il lume intestinale ma interagiscono con recettori immunitari mucosali,
modulando la produzione citochinica e supportando l’integrità epiteliale (Taverniti & Guglielmetti, 2011).
- Obiettivo funzionale: immunomodulazione mucosale con profilo di sicurezza elevato in contesti selezionati.
- Nota clinica: il razionale dipende dal ceppo e dalla tecnologia di inattivazione.
Implicazioni cliniche per il Biologo Nutrizionista
In una prospettiva applicativa, la valutazione funzionale dell’intestino dovrebbe considerare:
- Microbiota intestinale: diversità e funzioni (con attenzione ai metaboliti come gli SCFA).
- Muco intestinale: integrità dello strato mucoso e tolleranza alle fibre fermentabili.
- Tight junctions: segnali indiretti di aumentata permeabilità e fattori che possono comprometterle (stress, dieta, farmaci, infezioni).
- Immunità mucosale: indicatori clinici di dis-regolazione immunitaria e infiammazione persistente.
- Asse intestino-sistema: profilo metabolico e carico infiammatorio sistemico.
Principio operativo: i nutraceutici hanno maggiore coerenza clinica quando inseriti in un programma personalizzato che includa pattern alimentare, gestione dello stress, sonno e attività fisica.
Conclusioni
L’intestino emerge oggi come un organo regolatore sistemico, la cui funzionalità influenza molteplici assi fisiopatologici.
Più che origine universale delle malattie, esso rappresenta un nodo centrale di integrazione tra ambiente, nutrizione, immunità e metabolismo.
In questa cornice, il ruolo del biologo nutrizionista si configura come quello di interprete dell’ecosistema intestinale, chiamato a tradurre la complessità biologica in strategie nutrizionali personalizzate e basate su evidenze (Bischoff et al., 2014; Tilg & Moschen, 2014).
Nota informativa: il contenuto non sostituisce la valutazione clinica individuale. L’impiego di integratori/nutraceutici richiede personalizzazione, valutazione di tollerabilità, terapie in corso e possibili interazioni.
FAQ
Che cos’è la barriera intestinale?
La barriera intestinale è un sistema multistrato composto da microbiota, muco, epitelio con tight junctions e immunità mucosale.
Regola in modo selettivo il passaggio di nutrienti e limita la traslocazione di componenti microbiche (Bischoff et al., 2014; Turner, 2009).
Cos’è la permeabilità intestinale e perché è rilevante?
La permeabilità intestinale descrive l’aumento del passaggio paracellulare dovuto a disfunzione delle tight junctions.
Può favorire il passaggio di componenti microbiche (es. LPS) nel circolo, contribuendo a endotossiemia metabolica e infiammazione di basso grado (Cani et al., 2007).
Il butirrato è utile per la barriera intestinale?
Il butirrato rappresenta un substrato energetico per i colonociti e supporta la funzione di barriera, contribuendo al mantenimento delle tight junctions e alla modulazione immunitaria (Peng et al., 2009; Furusawa et al., 2013).
La berberina serve solo per la glicemia?
Oltre agli effetti metabolici, la berberina è studiata per proprietà antimicrobiche e antinfiammatorie, con potenziali effetti sulla modulazione del microbiota e di segnali associati all’endotossiemia metabolica (Habtemariam, 2020).
L’acido alfa-lipoico agisce direttamente sull’intestino?
L’acido alfa-lipoico non è un riparatore diretto della mucosa, ma può contribuire alla riduzione dello stress ossidativo sistemico, un fattore che può concorrere alla disfunzione della barriera in quadri selezionati (Packer et al., 1995).
Riferimenti bibliografici (selezione)
- Bischoff SC et al. (2014). Intestinal permeability and barrier function.
- Cani PD et al. (2007). Metabolic endotoxemia.
- Furusawa Y et al. (2013). Butyrate and Treg differentiation.
- Habtemariam S. (2020). Berberine pharmacology.
- Hotamisligil GS. (2006). Inflammation and metabolic disorders.
- Johansson MEV et al. (2013). Mucus barrier function.
- Kho ZY & Lal SK. (2018). Microbiome and immunity.
- Leone A et al. (2015). Moringa bioactive compounds.
- Mowat AM & Agace WW. (2014). GALT immunity.
- Packer L et al. (1995). Alpha-lipoic acid antioxidant role.
- Peng L et al. (2009). Butyrate and tight junctions.
- Playford RJ et al. (2001). Colostrum and gut permeability.
- Taverniti V & Guglielmetti S. (2011). Paraprobiotics.
- Tilg H & Moschen AR. (2014). Microbiota and inflammation.
- Turner JR. (2009). Intestinal tight junctions.
